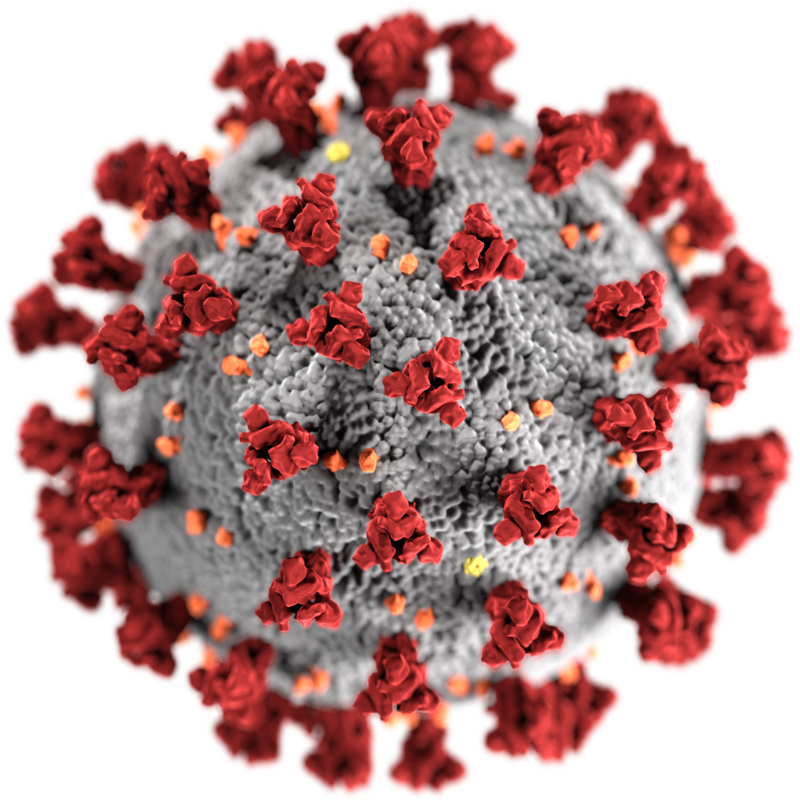
I Virus e possibile trattamento di patologie dovute a COVID 19
Nel gennaio 2020 inizia in Italia una epidemia dovuta a contagio di un corona virus inizialmente sconosciuto, ma con propagazione veloce e portando patologie polmonari molto spesso letali. Non sono qui a comprenderne la causa o se vi sia stata mutazione, fuga accidentale o contaminazione progettata, argomento di un successivo manoscritto . Molti propongono trattamenti con farmaci antivirali in commercio in Italia o altri Paesi come Russia o Giappone mostrando risultati miracolosi. Mi propongo di suggerire un trattamento alternativo con vitamina C endovena ad alte dosi oppure con due vitamine a alte dosi, vitamina C e B6, due vitamine idrosolubili indispensabili per la vita a basse dosi e possibili cure a elevate dosi endovena come noto in passato per malattie virali (Poliomelite). Tale approfondimento viene proposto con introduzione sui virus e successivamente sul COVID 19 e sviluppando letteratura scientifica dove sono stati riportate proprietà biochimiche e risultati clinici.
INTRODUZIONE
Virus è un termine latino che significa VELENO [1]. Esso è un sistema complesso con modalità di azione e attività compatibile con i parassiti. Analizzando la sua fisionomia il virus assomiglia a una cellula mancata infatti da un filamento centrale una singola o doppia elica di RNA o DNA protetto da un sistema proteico detto capside avente compito di protezione dalle nucleasi [Figura 1]. In alcuni casi il capside è avvolto in una membrana esterna detta peplo, o envelope o pericapside con composizione variabile di carboidrati, lipidi e proteine osservabili nell’herpesvirus, poxvirus e orthomyxovirus [2]. Essi sono sistemi acellulari e parassiti obbligati nell’ambito del loro ciclo vitale si svolge penetrando all’interno delle cellule. Ogni virus svolge la propria attività rigenerativa in specifici sistemi, per esempio alcuni agiscono nelle cellule vegetali e solo in determinate specie, altre in generale nei mammiferi, uccelli, batteri ecc.
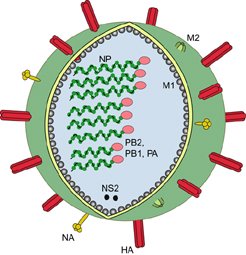
Figura 1 – Virione di virus influenzale -Von Dr. Influensa in der Wikipedia auf Norwegisch, CC BY-SA 2.5,
httpscommons.wikimedia.orgwindex.phpcurid=2850213
Tra i virus agenti sui mammiferi molti sono specifici per le cellule eucariotiche umane. Le infezioni virali possono causare patologie e verificarsi cambiamenti genetici. I virus specifici per i batteri detti batteriofagi [Figura 2] si legano a recettori specifici sulla membrana per poi entrare nel batterio. In primis l’enzima polimerasico batterico inizia la traduzione di mRNA batterico producendo proteine che serviranno al virus nel ciclo di attività. Successivamente avverranno una serie di copie del genoma virale iniziale e la biosintesi di enzimi per la protezione e infine la morte del batterio e la fuoriuscita dei batteriofagi [3].
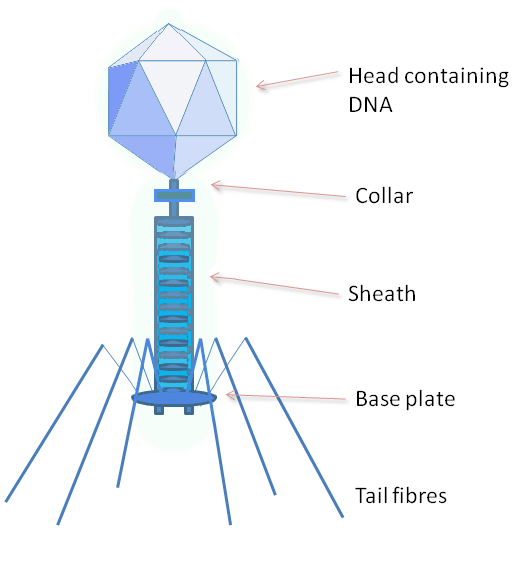
Figura 2 – struttura di un batteriofago – Di GrahamColm di Wikipedia in inglese, CC BY-SA 3.0,
httpscommons.wikimedia.orgwindex.phpcurid=7306290
Questo semplice esempio serve per la comprensione del ciclo dei virus aventi in comune le seguenti fasi:
1) Attaccamento ( fase in cui la parte terminale di proteine del capside virale si legano con proteine di membrana della cellula infettata);
2) Ingresso (fase successiva all’attaccamento dove il virione attraversa la membrana citoplasmatica della cellula per endocitosi per fusione di membrane o mediata da recettori. In alcuni casi il genoma può essere iniettato dall’esterno.);
3) Uncoating (fase successiva all’ingresso del virione nel citoplasma della cellula infettata e viene rilasciato il genoma e degradato il capside per effetto di enzimi virali o della cellula infettata);
4) Replicazione (fase successiva all’Uncoating dove il genoma si duplica n volte per effetto di enzimi specifici);
5) Assemblaggio ( fase il cui i nuovi genomi riformano capside tramite enzimi virali. Nel caso di HIV questa fase avviene dopo il rilascio);
6) Rilascio ( fase successiva all’assemblaggio e avviene la morte cellulare per lisi, liberando i nuovi virus).
Variabilità genomica del virus
La deriva antigenica è una modalità di mutazione genetica del virus. In particolare, variano singole basi nel genoma e spesso non conduce a variazioni di proteine codificate e tale fenomeno è chiamato “mutazione puntiforme silenziosa”. In altre occasioni la mutazione si oppone al farmaco antivirale creando virioni resistenti. La ricombinazione e riassortimento sono i modi di mutazione naturali [4-5]. La ricombinazione e riassortimento sono i modi di mutazione naturali e quando accade con i virus influenzali si verificano pandemie. I virus influenzali esistono spesso come sciami di virus della stessa specie ma con genoma leggermente diverso. Quando nel ciclo virale il genoma in costruzione si combina con pezzetti di altro genoma presente avviene la ricombinazione e il risultato è un virus figlio o offspring con genoma diverso, fenomeno detto riassortimento. Lo stesso effetto mutante può essere creato in laboratorio. La replicazione dei virus a DNA avviene generalmente nel nucleo della cellula infettata e utilizza strumenti molecolari della cellula, talvolta anche i propri; i virus a RNA promuovono usualmente la loro azione biologica nel citoplasma utilizzando enzimi propri per replicazione del genoma detti RNA replicasi. I retrovirus effettuano il loro ciclo biologico nel citoplasma come i virus a RNA.

Figura 3 – schema di come i diversi ceppi influenzali possano ricombinarsi creando ceppi completamente nuovi, con forma e caratteristiche d’entrambi. Questo processo è chiamato shift genetico ed è distinto dalla deriva genetica, che è il processo di accumulo di mutazioni puntiformi. Di Umberto NURS – Questo file deriva da: Influenza geneticshift.jpg:Jiver, CC BY-SA 4.0, https://commons.wikimedia.org/w/index.php?curid=43904121
In genere si lega alla cellula bersaglio tramite una glicoproteina ed entra per fusione con la membrana liberando capside contenente genoma. I retrovirus hanno genoma formato da due catene di RNA identiche. I genomi virali possono essere suddivisi in tre generiche parti :
1) gag codificante le proteine strutturali;
2) pol codificante le trascrittasi inverse e integrasi o replicasi o DNA polimerasi;
3) env codificante le proteine del pericapside.
Nel retrovirus il genoma liberato, tramite trascrittasi inversa, codifica segmento DNA a doppia elica tramite tRNA specifico del virione e tramite enzima integrasi il DNA prodotto si integra con la cellula infettata. Si rigenera genoma, capside e pericapside e per gemmazione vengono rilasciati dalla cellula [6-8]. Spesso l’infezione virale conduce al suicidio della cellula per apoptosi, atto estremo per fermare la replicazione virale non avendo altre possibilità di difesa [9]. I virus benchè siano i sistemi biologici più abbondanti sulla Terra possono variare rispetto alla loro composizione naturale per effetto di mutazioni spontanee aventi però bassissima probabilità oppure con attività biotecnologica di laboratorio , quindi possono essere facilmente sintetizzati e nel 2002 abbiamo notizia del primo virus artificiale [10-12]. In laboratorio è opportuno sintetizzare il genoma DNA (per virus a DNA) o cDNA (per virus a RNA) e messo all’interno della cellula affinché produca sé stesso in modo completo. Le sequenze genomiche di migliaia di virus sono contenute nel National Institutes of Health [13]. Dalle esperienze di pandemie avvenute nella storia, si prende il pessimo esempio di utilizzare sistemi virali quali possibili armamenti benchè vietati dall’ONU. Oggi il COVID 19 , un virus appartenente all’Ordine dei Nidovirales [14 -15] , famiglia coronoviridae [16-17], sottofamiglia dei Coronavirus [Figura 4] è acronimo dell’inglese COronaVIrus Disease 19 talvolta detta malattia respiratoria acuta da SARS-CoV-2 [18].
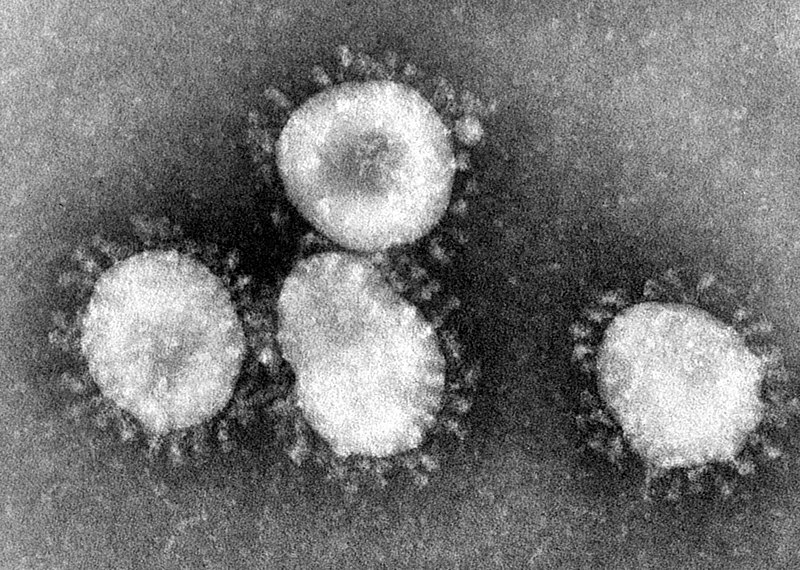
Figura 4 – Coronaviruses are a group of viruses that have a halo, or crown-like (corona) appearance when viewed under
an electron microscope. The coronavirus is now recognized as the etiologic agent of the 2003 SARS outbreak.
Additional specimens are being tested to learn more about this coronavirus, and its etiologic link with Severe
Acute Respiratory Syndrome. It is stated on the CDC website for a coloured version of the image that this
depicts the (Avian) Infectious bronchitis virus – Di Photo Credit:Content Providers(s): CDC/Dr. Fred Murphy –
This media comes from the Centers for Disease Control and Prevention’s Public Health Image Library (PHIL),
with identification number #4814.Note: Not all PHIL images are public domain; be sure to check copyright status and credit authors and content providers., Pubblico dominio, https://commons.wikimedia.org/w/index.php?curid=822112
Il COVID 19 [Figura 5] colpisce principalmente l’apparato respiratorio [19] ma può provocare una serie di sintomi come febbre, tosse, respiro corto, dolore ai muscoli, stanchezza e disturbi gastrointestinali quali la diarrea; nei casi più gravi può verificarsi una polmonite, una sindrome da distress respiratorio acuto, sepsi e shock settico, fino ad arrivare al decesso del paziente [20-21]. le principali modalità di trasmissione avvengono tra individui a stretto contatto per effetto di particelle di saliva dopo avere tossito o starnutito.

Figura 5 – This illustration, created at the Centers for Disease Control and Prevention (CDC), reveals ultrastructural morphology exhibited by coronaviruses. Note the spikes that adorn the outer surface of the virus, which impart the look of a corona surrounding the virion, when viewed electron microscopically. A novel coronavirus, named Severe Acute Respiratory Syndrome coronavirus 2 (SARS-CoV-2), was identified as the cause of an outbreak of respiratory illness first detected in Wuhan, China in 2019. The illness caused by this virus has been named coronavirus disease 2019 – Di CDC/ Alissa Eckert, MS; Dan Higgins, MAM – This media comes from the Centers for Disease Control and Prevention’s Public Health Image Library (PHIL), with identification number #23312.Note: Not all PHIL images are public domain; be sure to check copyright status and credit authors and content providers., Pubblico dominio, https://commons.wikimedia.org/w/index.php?curid=86444014
individui a stretto contatto per effetto di particelle di saliva dopo avere tossito o starnutito. La trasmissione può avvenire tra due persone una delle quali con patologia oppure asintomatico. È attualmente in corso la sperimentazione per verificare trasmissione per contatto con superfici contaminate dal COVID 19. Sono stati effettuati campioni anche sulle feci risultando positive circa metà delle persone con patologia in fase avanzata [22]. Nella saliva il virus rimane attivo qualche ora mentre sulle superfici per alcuni giorni [23-24]. Il COVID 19 risulterebbe derivare dalla ricombinazione del coronavirus del pipistrello e un virus sconosciuto e talvolta ipotizzato essere di origine naturale senza poter escludere origine di ingegneria genetica [25]. Osservo personalmente una serie di pubblicazioni dove gli autori affermano con certezza di una origine naturale del virus [26-28]. Benchè mutazioni e la combinazione tra due virus siano possibili, la probabilità è estremamente bassa, rispetto a una costruzione in laboratorio dove la probabilità è 100%. La sede più probabile è quella dove è stato studiato il virus della SARS e nella ricerca del vaccino con inquinamento dovuto a un virus del raffreddore. La probabilità maggiore è evidente se ottengo un corona virus e tramite gli spike terminali (antenne) potrebbe essere influenzato da campi magnetici statici e variabili l’attaccamento ai recettori cellulari cellula potendo in quel modo determinare la virulenza e quindi alla comunità contaminata. Se il COVID 19 ha espressione genomica responsabile della variabilità continua con efficacia di attacco e di mimetizzazione determinando patologie gravi, è ideale per rendere inefficace nemici in tempi rapidi e con inizio dopo 14 giorni dal contagio non dà sospetti per visite bilaterali e se infine potrà legarsi agli individui desiderati sarà il virus ideale per la guerra [29-30].
Vitamina C
I trattamenti dell’infezione, al momento vengono fatti curando sintomatologie oppure con antivirali e altri farmaci di norma utilizzati per altre patologie. Gli effetti di antivirali sul mercato italiano e estero sono in via di sperimentazione da parte di strutture ospedaliere. Da biochimico propongo di affrontare i soggetti contagiati con semplici vitamine idrosolubili: Vitamina C e B6. Pauling dimostrò una diminuzione del 15 – 20% di soggetti con raffreddore o influenza stagionale con integrazione di vitamina C da 200 mg/die fino a 1 g/die. Quindi una normale integrazione orale di acido ascorbico è in grado di ridurre l’avvenire della patologia per circa il 15% dei soggetti [31-32] Inoltre, è possibile effettuare esperimenti integrando vitamina C ad alte dosi contemporaneamente via orale e aumenta l’efficacia rispetto alla diminuzione dell’insorgenza di raffreddori e influenze endovena fino a 90 grammi complessivi come sostenevano Frederick Robert Klenner, Robert Cathcart e Linus Pauling in esperienze e pubblicazioni effettuate tra il 1974 e il 1992 per la cura di tutte le infezioni virali e altri proposti in esperimenti moderni [33-44]. Inoltre, riduce drasticamente la tossicità dovuta a altri farmaci [45-46]. È importante sottolineare l’utilizzo della vitamina C ad alte dosi per trattamenti a varie forme tumorali e altro da 600 mg a 90 grammi complessivi al giorno [47-61].
La vitamina B6
La vitamina B6 [62] è idrosolubile e essenziale pe la vita e viene reperita dall’organismo dei mammiferi tramite la dieta e all’attività batterica intestinale. Le sue forme in natura sono molteplici, piridossina, piridossale, piridossammina, le forma monofosfate in posizione 5’ e agliconi di zuccheri semplici o complessi [63-64]. È stata oggetto di interesse di numerosi esperimenti, alcuni dei quali in alte dosi orale e endovena. La piridossina ha la facoltà di inibire enzimi polimerasi e topoisomerasi [65-76] e conseguentemente potenziale bloccante di attività virale lasciando all’acido ascorbico di comportarsi da proosidante nelle cellule infettate, liberando acqua ossigenata, senza scalfire le cellule sane. La vitamina B6 come avviene per l’acido ascorbico è un antitumorale preventivo e soppressore [77-99].
Proposte terapeutiche
1) La presente proposta prevede assunzione orale di acido ascorbico e endovena con flebo di soluzione fisiologica: 5 grammi suddivisi nella giornata e 45 grammi endovena da raggiungere in tre giorni e studiando effetti e tolleranza del paziente. È possibile utilizzare 90 grammi al giorno come affermava Linus Pauling. Verifiche da fare sono pH della soluzione da iniettare endovena e dovrà avere valori compresi tra 7,30 e 7,35 (pH fisiologico).
2) La seconda proposta prevede tutta la prima parte con aggiunta di 600 mg al giornodi piridossina da iniettare endovena arrivando a tali valori in due giorni e con valori ematici elevati di acido ascorbico. Qualora il paziente infettato da COVID 19 non abbia effetti collaterali aumentare di 100 mg di vitamina B6 fino al massimo possibile di tolleranza che grazie alla presenza di acido ascorbico aumenterà notevolmente.
Eventi precedenti di utilizzo protocollo 1
Il Dr Domenico Mastrangelo è un medico ematologo specializzato in oncologia che lavora presso il policlinico Le Scotte di Siena. Esso ha utilizzato alte dosi di acido ascorbico per la cura del retinoblastoma ai fanciulli con risultati eccellenti e senza usare chemioterapici e suggerisco di contattarlo [100- 103]. Mi permetto un’ultima considerazione, Siena conta suicidi che talvolta non sono tali, lascio al buonsenso di ognuno ogni considerazione, poiché se non fosse così nel caso del Professore Francesco Lo Coco, sarebbe fonte di prova del funzionamento di sostanze efficaci a basso costo [104]. L’idea di utilizzare acido ascorbico e piridossina per sconfiggere il COVID 19 nasce sia dalla ottima bibliografia che evidenzia le proprietà eccezionali di queste due molecole ma anche da esperienze personali di utilizzo dello stesso a alte dosi e la morte del professore Lo Coco mi ha convinto definitivamente del quale spero si possa effettuare approfondimenti d’indagine.
Dr. Riccardo Zanaboni (Comitato Scientifico del C.I.R. Centro Italiano Ricerche)
°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
BIBLIOGRAFIA
[1] https://it.wikipedia.org/wiki/Virus_(biologia)#CITEREFShors;
[2] http://www.microbiologia.unige.it/dpb/Appunti/VIRUS1.pdf;
[3] https://www.chimica-online.it/biologia/virus.htm;
[4] Worobey M, Holmes EC, Evolutionary aspects of recombination in RNA viruses, in J. Gen. Virol., 80 ( Pt 10),
1999, pp. 2535–43, PMID 10573145;
[5] Bentley K, Evans DJ. Mechanisms and consequences of positive-strand RNA virus recombination. .J Gen
Virol. 2018 Oct;99(10):1345-1356. doi: 10.1099/jgv.0.001142. Epub 2018 Aug 29.PMID: 30156526;
[6] https://www.chimica-online.it/biologia/retrovirus.htm;
[7] Staginnus C, Richert-Pöggeler KR, Endogenous pararetroviruses: two-faced travelers in the plant genome,
in Trends in Plant Science, vol. 11, nº 10, 2006, pp. 485–91, DOI:10.1016/j.tplants.2006.08.008,
[8 ] Leslie Collier, Albert Balows e Max Sussman, Virology, in Brian H Mahy e Leslie Collier (a cura di), Topley
and Wilson’s Microbiology and Microbial Infections, vol. 1, 9ª ed., Arnold, 1998, ISBN 0-340-66316-2;
[9] Roulston A, Marcellus RC, Branton PE, Viruses and apoptosis, in Annu. Rev. Microbiol., vol. 53, 1999, pp. 577–
628, DOI:10.1146/annurev.micro.53.1.577;
[10] Cello J, Paul AV, Wimmer E, Chemical Synthesis of poliovirus cDNA: generation of infectious virus in the absence of natural template. Science, vol. 297, nº 5583, 2002, pp. 1016–8, Bibcode: 2002 Sci…297.1016C, DOI:10.1126/science.1072266, PMID 12114528;
[11] Coleman JR, Papamichail D, Skiena S, Futcher B, Wimmer E, Mueller S, Virus attenuation by genome-
scale changes in codon pair bias. Science, vol. 320, nº 5884, 2008, pp. 1784-7 Bibcode:
2008Sci…320.1784C, DOI:10.1126/science.1155761, PMC 2754401, PMID 18583614;
[12] Wen AM, Steinmetz NF. Design of virus-based nanomaterials for medicine, biotechnology, and energy.
Chem Soc Rev. 2016 Jul 25;45(15):4074-126. doi: 10.1039/c5cs00287g. PMID: 27152673; PMCID:
PMC5068136;
[13] Genomes, NIH viral genome database, su ncbi.nlm.nih.gov. URL consultato il 19 dicembre 2014
[14] https://it.wikipedia.org/wiki/Nidovirales;
[15] Cavanagh D. «Nidovirales: a new order comprising Coronaviridae and Arteriviridae». Arch Virol. 1997;
142(3):629-33, PMID 9349308;
[16] https://en.wikipedia.org/wiki/Coronaviridae;
[17] McBride, Ruth; van Zyl, Marjorie; Fielding, Burtram C. (7 August 2014). “The Coronavirus Nucleocapsid Is a
Multifunctional Protein”. Viruses. 6 (8): 2991–3018.
[18] Accademia della Crusca, NOTA per la redazione: CoViD 19 (abbreviazione di coronavirus disease 19) è la
denominazione della malattia respiratoria causata dal virus SARS-CoV-2; nel primo caso si usa l’articolo
determinativo femminile, nel secondo caso quello maschile., su @AccademiaCrusca, 8 marzo 2020. URL
consultato il 15 marzo 2020;
[19] Matthay, Michael A.; Aldrich, J. Matthew; Gotts, Jeffrey E. (March 2020). “Treatment for severe acute respiratory
distress syndrome from COVID-19”. The Lancet Respiratory Medicine.
doi:10.1016/S2213-2600(20)30127-2. PMID 32203709
[20] https://www.who.int/health-topics/coronavirus#tab=tab_3
[21] Wei-jie Guan, Ph.D., Zheng-yi Ni, M.D., Yu Hu, M.D., Wen-hua Liang, Ph.D., Chun-quan Ou, Ph.D., Jian-xing He,
M.D., Lei Liu, M.D., Hong Shan, M.D., Chun-liang Lei, M.D., David S.C. Hui, M.D., Bin Du, M.D., Lan-juan Li,
M.D., et al., for the China Medical Treatment Expert Group for Covid-19* Clinical Characteristics of
Coronavirus Disease 2019 in China – The New England Journal of Medicine – February 28, 2020
DOI: 10.1056/NEJMoa2002032;
[22] Jinyang Gu, Bing Han e Jian Wang, COVID-19: Gastrointestinal manifestations and potential fecal-oral
transmission, in Gastroenterology, 2020-03, DOI:10.1053/j.gastro.2020.02.054;
[23] “Coronavirus Disease 2019 (COVID-19) – Transmission”. Centers for Disease Control and Prevention. 17
March 2020. Retrieved 23 March 2020;
[24] “New coronavirus stable for hours on surfaces”. National Institutes of Health. 17 March 2020. Retrieved 23
March 2020.
[25] http://theconversation.com/coronavirus-origins-genome-analysis-suggests-two-viruses-may-have-combined-134059
[26] Andersen, K.G., Rambaut, A., Lipkin, W.I. et al. The proximal origin of SARS-CoV-2. Nat Med (2020).
https://doi.org/10.1038/s41591-020-0820-9;
[27] Tao Zhang, Qunfu Wu , Zhigang Zhang – Probable Pangolin Origin of SARS-CoV-2 Associated with the
COVID-19 Outbreak – Current Biology – 2020 in press;
[28] Syed Faraz Ahmed, Ahmed A. Quadeer and Matthew R.Mckay – Preliminary Identification of Potential
Vaccine Targets for the COVID-19 Coronavirus (SARS-CoV-2) Based on SARS-CoV Immunological Studies –
Viruses 2020, 12(3), 254; https://doi.org/10.3390/v12030254;
[29] Franco Cataldo – Lezioni sulle armi chimiche , biologiche e nucleari e relativa protezione –
2004 – Società Lupi arl Editore – Roma.
[30] Franco Angeli – Veleni di guerra in tempo di pace – 2003 – Collana Pometheus fondata da
Paolo Bisogno;
[31] Stefano Pravato – Guarire con la Vitamina C – Malattie curate, effetti benefici, tipologie e
modalità di assunzione – 2013 – Macro Edizioni – Cesena (FC);
[32] Linus Pauling – Vitamin C and the common cold – 1970 – W.H. Freeman and Company – San
Francisco
[33] Ely JT. Ascorbic acid role in containment of the world avian flu pandemic. Exp Biol Med
2007; 232(7): 847-51
[34] Michael J Gonzalez, Miguel J Berdiel, Jorge Duconge, Thomas E Levy, Ines M Alfaro, Raul
Morales-Borges, Victor Marcial-Vega, Jose Olalde; High Dose Intravenous Vitamin C and
Influenza: A Case Report – Journal of Orthomolecular Volume 34, Number 2, 2019
[35] Thompson WW, Shay DK, Weintraub E, Brammer L, Cox N, Anderson LJ, Fukuda K. Mortality associated
with influenza and respiratory syncytial virus in the United States. JAMA, 2003;289(2):179-86.
[36] S Harakeh, R J Jariwalla, and L Pauling – Suppression of human immunodeficiency virus replication by
ascorbate in chronically and acutely infected cells. Proc Natl Acad Sci U S A. 1990 Sep; 87(18): 7245–
7249.doi: 10.1073/pnas.87.18.7245
[37] Murata A, Uike M. Mechanism of inactivation of bacteriophage MS2 containing single-stranded RNA by
ascorbic acid. J Nutr Sci Vitaminol (Tokyo) 1976;22(5):347–354
[38] Schwerdt PR, Schwerdt CE. Effect of ascorbic acid on rhinovirus replication in WI-38 cells. Proc Soc Exp Biol
Med. 1975 Apr;148(4):1237–1243;
[39] Bissell MJ, Hatie C, Farson DA, Schwarz RI, Soo WJ. Ascorbic acid inhibits replication and
infectivity of avian RNA tumor virus. Proc Natl Acad Sci U S A. 1980 May;77(5):2711–2715;
[40] Takuma Hayash – Preventive Effect of Ascorbic Acid Against Biological Function of Human
Immunodeficiency Virus Trans Activator of Transcription – J Intercult Ethnopharmacol
, 5 (2), 205-9 2016 Apr 6 eCollection Mar-Apr 2016;
[41] Liang WJ, Johnson D, Jarvis SM. Vitamin C transport systems of mammalian cells. Mol Membr Biol.
2001;18:87–95;
[42] Moens, B., Decanine, D., Khouri, R. et al. Ascorbic acid has superior antiviral and antiproliferative effects
over IFN-alpha in HAM/TSP PBMC ex vivo. Retrovirology 8, A61 (2011). https://doi.org/10.1186/1742-
4690-8-S1-A61;
[43] Ruben Manuel Luciano Colunga Biancatelli, Max Berrill & Paul E. Marik (2020) The antiviral properties of
vitamin C, Expert Review of Anti-infective Therapy, 18:2, 99-101, DOI: 10.1080/14787210.2020.1706483;
[44] Jariwalla R.J., Harakeh S. (1996) Antiviral and Immunomodulatory Activities of Ascorbic Acid. In: Harris J.R.
(eds) Subcellular Biochemistry. Subcellular Biochemistry (Ascorbic Acid: Biochemistry and Biochemical Cell
Biology), vol 25. Springer, Boston, MA;
[45] Yan Ma, Julia Chapman, Mark Levine, Kishore Polireddy, Jeanne Drisko, Qi Chen – High-Dose Parenteral
Ascorbate Enhanced Chemosensitivity of Ovarian Cancer and Reduced Toxicity of Chemotherapy – Science
Translational Medicine 05 Feb 2014: Vol. 6, Issue 222, pp. 222ra18 – DOI: 10.1126/scitranslmed.3007154;
[46] Conclusion on the peer review of the pesticide risk assessment of the active substance L-ascorbic acid1
European Food Safety Authority2 European Food Safety Authority (EFSA), Parma, Italy- EFSA Journal
2013;11(4):3197;
[47] Ruichuan Yin, Shi-Qing Mao, Bailin Zhao, Zechen Chong, Ying Yang, Chao Zhao, Dapeng Zhang
Hua Huang, Juan Gao, Zheng Li, Yan Jiao, Cuiping Li, Shengquan Liu,Danni Wu, Weikuan Gu, Yun-Gui Yang,
Guo-Liang Xu, Hailin Wang – Ascorbic Acid Enhances Tet-Mediated 5-Methylcytosine Oxidation and
Promotes DNA Demethylation in Mammals – J. Am. Chem. Soc. 2013, 135, 28, 10396-10403Publication
Date:June 14, 2013 -https://doi.org/10.1021/ja4028346;
[48] D. Mastrangelo, T. Hadjistilianou, S. De Francesco and C. Loré, “Retinoblastoma and the Genetic Theory of
Cancer: an Old Paradigm Trying to Survive to the Evidence,” Journal of Cancer Epidemiology, Vol. 2009,
2009. doi:10.1155/2009/301973;
[49] Abel Ang, Juliet M. Pullar, Margaret J. Currie, Margreet C.M. Vissers; Vitamin C and immune cell function in
inflammation and cancer. Biochem Soc Trans 19 October 2018; 46 (5): 1147–1159.
doi: https://doi.org/10.1042/BST20180169
[50] Ana S. Pires, Cláudia R. Marques1,2, João C. Encarnação1,3, Ana M. Abrantes1,3, Inês A. Marques1,3, Mafalda
Laranjo1,3, Rui Oliveira1,3,4, João E. Casalta-Lopes1,3, Ana C. Gonçalves3,5, Ana B. Sarmento-Ribeiro3,5,6
and Maria F. Botelho – Ascorbic Acid Chemosensitizes Colorectal Cancer Cells and Synergistically Inhibits
Tumor Growth – Front. Physiol., 23 July 2018 | https://doi.org/10.3389/fphys.2018.00911
[51] Chen, Q., Espey, M. G., Krishna, M. C., Mitchell, J. B., Corpe, C. P., Buettner, G. R., et al. (2005). Pharmacologic
ascorbic acid concentrations selectively kill cancer cells: action as a pro-drug to deliver hydrogen peroxide
to tissues. Cell 102, 13604–13609. doi: 10.1073/pnas.0506390102;
[52] Fukui, M., Yamabe, N., Choi, H.-J., Polireddy, K., Chen, Q., and Zhu, B. T. (2015). Mechanism of ascorbate-
induced cell death in human pancreatic cancer cells: Role of Bcl-2, Beclin 1 and autophagy. Planta Med. 81,
838–846. doi: 10.1055/s-0035-1546132;
[53] Riordan, N. H., Riordan, H. D., Meng, X., Li, Y., and Jackson, J. A. (1995). Intravenous ascorbate as a tumor
cytotoxic chemotherapeutic agent. Med. Hypotheses 44, 207–213. doi: 10.1016/0306-9877(95)90137-X;
[54] Serrano, O. K., Parrow, N. L., Violet, P.-C. C., Yang, J., Zornjak, J., Basseville, A., et al. (2015). Antitumor effect
of pharmacologic ascorbate in the B16 murine melanoma model. Free Radic. Biol. Med. 87, 193–203.
doi:10.1016/j.freeradbiomed.2015.06.03;
[55] Domenico Mastrangelo, Lauretta Massai, Giuseppe Fioritoni and Francesco Lo Coco – High Doses of Vitamin
C and Leukaemia: In Vitro Update.2017 – Advances Leuk Res Treat 1(1):5-19 – REVIEW ARTICLE | VOLUME
1 | ISSUE 1 | DOI: 10.36959/486/323;
[56] Domenico Mastrangelo, Lauretta Massai – High doses of ascorbate (vitamin c): a new frontier in the
treatment of intraocular cancer – Adv Ophthalmol Vis Syst. 2016;4(1):1-6.
DOI: 10.15406/aovs.2016.04.00090;
[57] Domenico Mastrangelo, Lauretta Massai , Leda Lodi, Mariamichela Muscettola, Giovanni Grasso
Vitamina C ad alte dosi nel trattamento del cancro: un’ipotesi suggestiva del trattamento del cancro:
un’ipotesi suggestiva – Divisione di Scienze Biomediche Dipartimento di Scienze Mediche Chirurgiche e
Neuroscienze Università degli Studi di Siena – M.D. Medicina e Doctor – Anno XXI numero 5 – giugno/luglio
2014;
[58] Jeanne A. Drisko , Oscar K. Serrano, Lisa R. Spruce, Qi Chen and Mark Levinee – Treatment of pancreatic
cancer with intravenous vitamin C: a case report – Anticancer Drugs. 2018 Apr; 29(4): 373–379.
[59] Michael J. González , Miguel J. Berdiel, Jorge R Miranda-Massari, Desireé López, Jorge Duconge,
Joshua L. Rodriguez, Pedro Adrover – Integr Cancer Sci Therap – 2016 – Volume 3(6): 1-2
doi: 10.15761/ICST.1000219;
[60] https://www.cancer.gov/about-cancer/treatment/cam/patient/vitamin-c-pdq
[61] Hitomi K., Tsukagoshi N. (1996) Role of Ascorbic Acid in Modulation of Gene Expression. In: Harris J.R. (eds)
Subcellular Biochemistry. Subcellular Biochemistry (Ascorbic Acid: Biochemistry and Biochemical Cell
Biology), vol 25. Springer, Boston, MA;
[62]P. Gyorgy – The history of vitamin B6 – Am.J.Clin. Nutr. – 1956 – 4(4):313-317;
[63] Ink SL, Henderson LM (1984). “Vitamin B6 metabolism”. Annual Review of Nutrition. 4: 455–70.
doi:10.1146/annurev.nu.04.070184.002323. PMID 6380540.
[64] Johansson S, Lindstedt S, Tiselius HG (October 1974). “Metabolic interconversions of different forms of vitamin
B6”. The Journal of Biological Chemistry. 249 (19): 6040–6. PMID 4418204.
[65] Miwa NAKARI, Hiroaki KANOUCHI, Tatsuzo OKA – High Dose of Pyridoxine Induces IGFBP-3 mRNA
Expression in MCF-7 Cells and Its Induction Is Inhibited by the p53-Specific Inhibitor Pifithrin-a – 2011 –
J.Nutr. Sci. Vitaminol 57, 280-284:
[66] Mukund J. Modak -Observations on the pyridoxal 5′-phosphate inhibition of DNA polymerases –
Biochemistry 1976 15 (16), 3620-3626 – DOI: 10.1021/bi00661a033;
[67] Alejandro Araya, Julie Labouesse, Simon Litvak – Primer tRNATrp enhances the inhibition of avian
myeloblastosis virus reverse transcriptase by pyridoxal-5′-phosphate – Biochemical and Biophysical
Research – Communications – Volume 88, Issue 1, 14 May 1979, Pages 9-15 ;
[68] Matsubara, K., Matsumoto, H., Mizushina, Y., Lee, J.S., & Kato, N. (2003). Inhibitory effect of pyridoxal 5′-
phosphate on endothelial cell proliferation, replicative DNA polymerase and DNA topoisomerase.
International Journal of Molecular Medicine, 12, 51-55. https://doi.org/10.3892/ijmm.12.1.51;
[69] Tiziana Bellini, Maurizio Tomasi, Franco Dallocchio – Selective modification of Sendai virus hemagglutinin
neuraminidase by pyridoxal 5′-phosphate: evidence for an allosteric modulation of neuraminidase activity –
Biochimica et Biophysica Acta (BBA) – Protein Structure and Molecular Enzymology -Volume 1161, Issues 2–
3, 13 February 1993, Pages 323-327 – https://doi.org/10.1016/0167-4838(93)90232-G;
[70] L Guo, N K Heinzinger, M Stevenson, L M Schopfer, J M Salhany – Inhibition of gp120-CD4 interaction and
human immunodeficiency virus type 1 infection in vitro by pyridoxal 5′-phosphate.Antimicrobial Agents and
Chemotherapy Oct 1994, 38 (10) 2483-2487; http//doi.org/10.1128/AAC.38.10.2483;
[71] T Oka, H Sugitatsu, H Nordina, M.K Thakur, M Aoyama, T Sasagawa, I Suzuki, T sujid – Pyridoxal 5′-phosphate
inhibits DNA binding of HNF1 – Biochimica et Biophysica Acta (BBA) – General Subjects – Volume 1568, Issue
3, 19 December 2001, Pages 189-196 – https://doi.org/10.1016/S0304-4165(01)00221-5 ;
[72] Mukund J.Modak – Pyridoxal 5′ phosphate: A selective inhibitor of oncornaviral DNA polymerases –
Biochemical and Biophysical Research Communications – Volume 71, Issue 1, 12 July 1976, Pages 180-187
https://doi.org/10.1016/0006-291X(76)90266-7 ;
[73] A Basu, R S Tirumalai and M J Modak – Substrate binding in human immunodeficiency virus reverse
transcriptase. An analysis of pyridoxal 5′-phosphate sensitivity and identification of lysine 263 in the
substrate-binding domain. – The Journal Of Biological Chemistry – Vol. 264, No. 15, Issue of May 25. pp.
8746 -8752;
[74] Alan Monaghan and Ronald T. Hay – Pyridoxal 5′-Phosphate Inhibition of Adenovirus DNA Polymerase – The
Journal Of Biological Chemistry – Vol. 271, No. 39, Issue of September 27, pp. 24242–24248, 1996 –
doi:10.1074/jbc.271.39.24242;
[75] Laura K. Moen, I. C. Bathurst, and P. J. Barr – Pyridoxal-5′-Phosphate Inhibits the Polymerase Activity of a
Recombinant RNase H-Deficient Mutant of HIV-1 Reverse Transcriptase – AIDS Research and Human
Retroviruses – .May 1992.597-604. http://doi.org/10.1089/aid.1992.8.597;
[76] Oh, S.-H., Park, Y.-H. and Woo, K. (1989) – Inactivation of human hepatitis b virus dna polymerase by pyridoxal
5′-phosphate. J. Med. Virol., 28: 42-46. https://doi.org/10.1002/jmv.1890280110;
[77] Galluzzi, L., Vacchelli, E., Michels, J. et al. Effects of vitamin B6 metabolism on oncogenesis, tumor progression
and therapeutic responses. Oncogene 32, 4995–5004 (2013). https://doi.org/10.1038/onc.2012.623;
[78] DiSorbo DM, Litwack G. Vitamin B6 kills hepatoma cells in culture. Nutr Cancer. 1982;3(4):216–222.
doi:10.1080/01635588109513725;
[79] DiSorbo DM, Paavola LG, Litwack G. Pyridoxine resistance in a rat hepatoma cell line. Cancer Res.
1982;42(6):2362–2370.
[80] Bessler H, Djaldetti M. Vitamin B6 Modifies the Immune Cross-Talk between Mononuclear and Colon
Carcinoma Cells. Folia Biol (Praha). 2016;62(1):47–52.
[81] Matsubara K, Komatsu S, Oka T, Kato N. Vitamin B6-mediated suppression of colon tumorigenesis, cell
proliferation, and angiogenesis (review). J Nutr Biochem. 2003;14(5):246–250. doi:10.1016/s0955-
2863(03)00009-3;
[82] Komatsu S, Yanaka N, Matsubara K, Kato N. Antitumor effect of vitamin B6 and its mechanisms. Biochim
Biophys Acta. 2003;1647(1-2):127–130. doi:10.1016/s1570-9639(03)00076-1;
[83] Komatsu S, Watanabe H, Oka T, Tsuge H, Kat N. Dietary vitamin B6 suppresses colon tumorigenesis, 8-
hydroxyguanosine, 4-hydroxynonenal, and inducible nitric oxide synthase protein in azoxymethane-treated
mice. J Nutr Sci Vitaminol (Tokyo). 2002;48(1):65–68. doi:10.3177/jnsv.48.65;
[84] Matsuo T, Sadzuka Y. In Vitro Anticancer Activities of B6 Vitamers: A Mini-review. Anticancer Res.
2019;39(7):3429–3432. doi:10.21873/anticanres.13488 ;
[85] Yanaka N, Kanda M, Toya K, Suehiro H, Kato N. Vitamin B6 regulates mRNA expression of peroxisome
proliferator-activated receptor-? target genes. Exp Ther Med. 2011;2(3):419–424. doi:10.3892/etm.2011.238
[86] Komatsu SI, Watanabe H, Oka T, Tsuge H, Nii H, Kato N. Vitamin B-6-supplemented diets compared with a low
vitamin B-6 diet suppress azoxymethane-induced colon tumorigenesis in mice by reducing cell proliferation.
J Nutr. 2001;131(8):2204–2207. doi:10.1093/jn/131.8.2204;
[87] Zhang X, Lee JE, Ma J, et al. Prospective cohort studies of vitamin B-6 intake and colorectal cancer incidence:
modification by time? – Am J Clin Nutr. 2012;96(4):874–881. doi:10.3945/ajcn.112.037267;
[88] Chou YC, Chu CH, Wu MH, et al. Dietary intake of vitamin B(6) and risk of breast cancer in taiwanese women.
J Epidemiol. 2011;21(5):329–336. doi:10.2188/jea.JE20100188;
[89] Shimada D, Fukuda A, Kawaguchi H, et al. Effect of high dose of pyridoxine on mammary tumorigenesis. Nutr
Cancer. 2005;53(2):202–207. doi:10.1207/s15327914nc5302_9;
[90] DiSorbo DM, Nathanson L. High-dose pyridoxal supplemented culture medium inhibits the growth of a human
malignant melanoma cell line. Nutr Cancer. 1983;5(1):10–15. doi:10.1080/01635588309513773;
[91] DiSorbo DM, Wagner R Jr, Nathanson L. In vivo and in vitro inhibition of B16 melanoma growth by vitamin
B6. Nutr Cancer. 1985;7(1-2):43–52. doi:10.1080/01635588509513838;
[92] Shultz TD, Santamaria AG, Gridley DS, Stickney DR, Slater JM. Effect of pyridoxine and pyridoxal on the in vitro
growth of human malignant melanoma. Anticancer Res. 1988;8(6):1313–1318;
[93] Gridley DS, Stickney DR, Nutter RL, Slater JM, Shultz TD. Suppression of tumor growth and enhancement of
immune status with high levels of dietary vitamin B6 in BALB/c mice. J Natl Cancer Inst. 1987;78(5):951–959.
[94] Molina A, Oka T, Munoz SM, Chikamori-Aoyama M, Kuwahata M, Natori Y. Vitamin B6 suppresses growth and
expression of albumin gene in a human hepatoma cell line HepG2. Nutr Cancer. 1997;28(2):206–211.
doi:10.1080/01635589709514576;
[95] Shimada D, Fukuda A, Kanouchi H, Matsumoto M, Oka T. Vitamin B6 suppresses growth of the feline mammary
tumor cell line FRM. Biosci Biotechnol Biochem. 2006;70(4):1038–1040. doi:10.1271/bbb.70.1038;
[96] Takeuchi PL, Antunes LM, Takahashi CS. Evaluation of the clastogenicity and anticlastogenicity of vitamin B6
in human lymphocyte cultures. Toxicol In Vitro. 2007;21(4):665–670. doi:10.1016/j.tiv.2007.01.004;
[97] Tryfiates GP, Morris HP, Sonidis GP. Vitamin B6 and cancer (review). Anticancer Res. 1981;1(5):263–267.
[98] Masaki Minamino, Tatsuzo Oka & Hiroaki Kanouchi (2015) Growth suppression and cell death by pyridoxal
is dependent on p53 in the human breast cancer cell line MCF-7, Bioscience, Biotechnology, and Biochemistry,
79:1, 124-129, DOI: 10.1080/09168451.2014.952618;
[99] Matsuo, T., Fujiwara, A., Nakamura , K., & Sadzuka, Y. (2018). The effects of vitamin B6 compounds on cell
proliferation and melanogenesis in B16F10 melanoma cells. Oncology Letters, 15, 5181-5184.
https://doi.org/10.3892/ol.2018.7947;
[100] https://www.omicsonline.org/abstract/the-anticancer-properties-of-vitamin-c-in-vitro-update/
[101] http://www.scienzemedicolegali.it/documenti/curriculum/cv-mastrangelo.pdf
[103] https://www.youtube.com/results?search_query=vitamina+c+and+cancro
Dr.Riccardo Zanaboni PhD
(Comitato Scientifico) C.I.R Centro Italiano Ricerche – Roma