Incremento dell’anidride carbonica sulla Terra
(Experimenta et Hypotheses Chemica)
Nell’atmosfera terrestre, la concentrazione dell’anidride carbonica ha raggiunto 410 ppm. Le conseguenze potrebbero essere molteplici. Siamo soliti associare la CO2 all’effetto serra e di conseguenza all’incremento della temperatura sulla Terra. Su questo argomento i pareri sono discordanti poichè molti scienziati pensano che l’incremento della temperatura sia dovuto prevalentemente a fenomeni astronomici. Un dato certo, invece, è dato dall’aumento della concentrazione di anidride carbonica nelle acque marine . L’aumento della concentrazione atmosferica e della pressione parziale procedono parallelamente. L’anidride carbonica è un gas che reagisce con l’acqua solo per lo 0,2% quindi, con buona approssimazione, può essere utilizzata la legge di Henry che stabilisce relazione tra la concentrazione di un gas non reagente col solvente e la pressione parziale a una data temperatura. In verità, circa lo 0,2% del biossido di carbonio reagisce con acqua per dare acido carbonico. Inoltre l’aumento della temperatura della massa di acqua di mare diminuisce la solubilità di anidride carbonica e degli altri gas come l’ossigeno, ma aumenta l’energia cinetica media delle molecole e ioni aumentando probabilità di urti efficaci e reazioni chimiche. In effetti stiamo assistendo a una diminuzione di pH nelle acque di mare e questo sembra dovuto a una reazione nella quale sarebbe coinvolta l’anidride carbonica. Nella figura 1 si osserva la reazione 1 nella quale si calcola la costante K che determina il rapporto tra la pressione parziale della CO2 sopra l’acqua e la concentrazione .
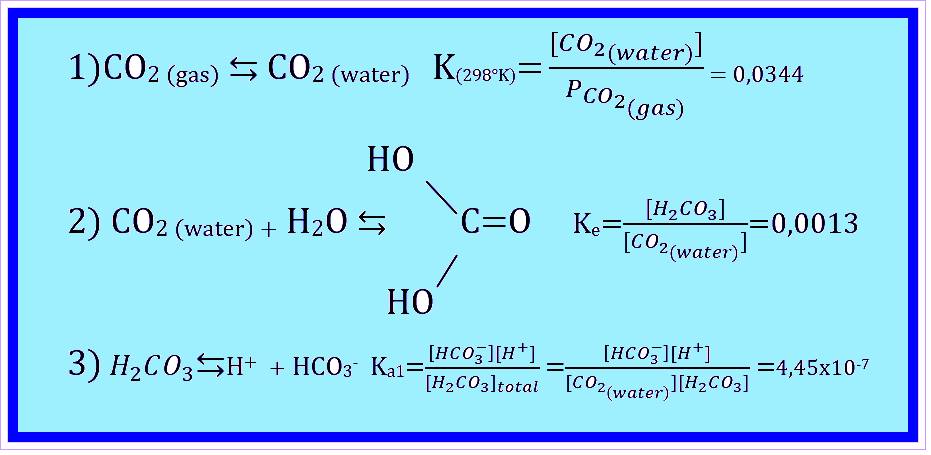
Figura_1 equilibri del biossido di carbonio in acqua.
Il valore 0,0344 è costante per ogni temperatura e se una parte di anidride carbonica nell’acqua di mare viene consumata a seguito di una reazione chimica, viene ripristinata dall’atmosfera soprastante.
La reazione 2 in figura 1 ci indica che solo circa lo 0,2% dell’anidride carbonica solubilizzata viene trasformata in acido carbonico che si dissocia in ione idrogeno e bicarbonato poichè il pH dell’acqua di mare è circa 8,10 e la costante Ka1= 4,45 x10^-7.
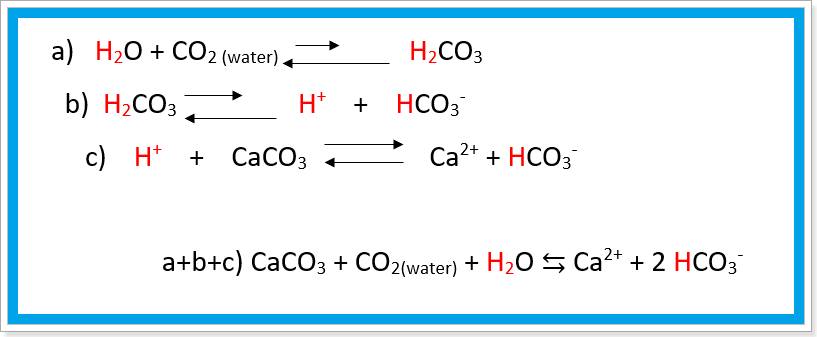
Figura_2 reazione tra il biossido di carbonio con il calcare.
La figura 2 mostra i passaggi a, b, c, a + b + c con conseguente solubilizzazione dei calcari nelle fattispecie di ioni calcio e bicarbonato. Le tendenza delle acque dei mari è l’incremento della Temperatura media e abbassamento del pH. Attualmente il pH = 8,10 con diminuzione di circa 0,25 unità rispetto al 1751 (periodo della rivoluzione industriale).
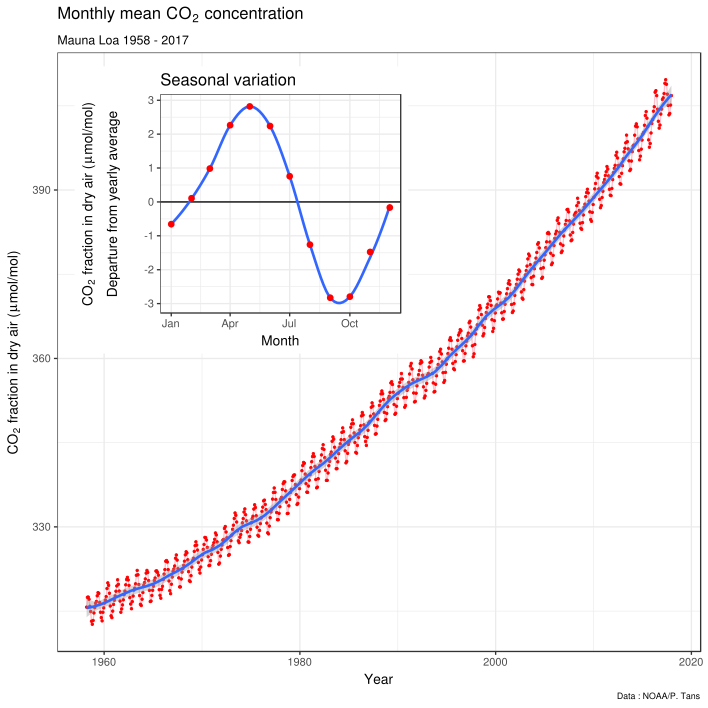
Figura_3 The Keeling Curve of atmospheric CO2 concentrations measured at Mauna Loa Observatory
Gli ecosistemi hanno la proprietà di opporsi a stress esterni (resistenza) e di ripristinare le condizioni iniziali (resilienza). Vorrei sperare che i limiti di irreversibilità non siano stati oltrepassati . Gli ecosistemi marini sono muniti di composti tampone e sono enormi serbatoi di calore in grado di regolare la temperatura del pianeta Terra. L’aumento della temperatura e l’abbassamento del pH conducono a incrementi di solubilità dei composti insolubili come alcuni idrossidi, carbonati e solfuri di elementi di transizione e del gruppo analitico II, III, IV e V.
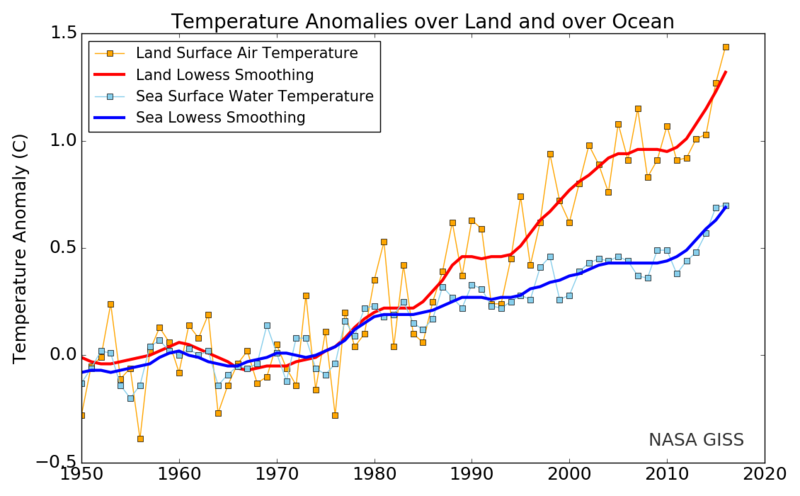
Figura_4 Annual (thin lines) and five-year lowess smooth ….
Increase of carbon dioxide on the Earth
In the Earth’s atmosphere, the concentration of carbon dioxide has reached 410 ppm. The consequences could be multiple. We usually associate CO2 with the greenhouse effect and consequently the increase in temperature on Earth. On this topic the opinions are discordant because many scientists think that the increase in temperature is mainly due to astronomical phenomena. A certain fact, however, is given by the increase in the concentration of carbon dioxide in marine waters too. The increase in atmospheric concentration and partial pressure proceed in parallel and though carbon dioxide is a gas that reacts with water. I will perform analysis using Henry’s law establishing relationship between the concentration of a unreacted gas and partial pressure at a given temperature. In truth, about 0.2% of carbon dioxide reacts with water in order to give carbonic acid. Furthermore, the increase temperature in seawater mass decreases the solubility of carbon dioxide and other gases such as oxygen, but increases the average kinetic energy of the molecules and ions, increasing the likelihood of effective impacts and chemical reactions. In fact we are seeing a decrease in pH in sea water and this seems to be due to a reaction in which carbon dioxide would be involved. Figure 1 shows the reaction 1 in which the constant K is calculated which determines the ratio between the partial pressure of CO2 above the water and the concentration.
The value 0.0344 is constant for each temperature and if a part of carbon dioxide in the sea water is consumed as a result of a chemical reaction, it is restored by the atmosphere above.
The reaction 2 in Figure 1 shows us that only about 0.2% of the solubilized carbon dioxide is transformed into carbonic acid which dissociates into hydrogen and bicarbonate ion since the pH of the sea water is about 8.10 and the constant Ka1 = 4.45 x 10 ^ -7. At this point, figure 2 shows the steps a, b, c separated and together with subsequent solubilization of the limestones in the species of calcium and bicarbonate ions. The tendency of the waters of the seas is an increase in the average temperature and lowering of the pH. Currently the pH = 8.10 with a decrease of about 0.25 units compared to 1751 (period of the industrial revolution).
Ecosystems have the property of opposing external stress (resistance) and restoring initial conditions (resilience). I would like to hope that the limits of irreversibility have not been exceeded. The marine ecosystems are equipped with buffer compounds and are huge reservoirs of heat that can regulate the temperature of the Earth. The increase in temperature and the lowering of the pH lead to increases in solubility of insoluble compounds such as some hydroxides, carbonates and sulfides of transition elements and of the analytical group II, III, IV and V.
Dr. Riccardo Zanaboni
(Esponente del Comitato Scientifico del C.I.R. Centro Italiano Ricerche)
Fonte Articolo:
————————————-
FONTI:
1)https://en.wikipedia.org/wiki/Sea_surface_temperature;
2)https://en.wikipedia.org/wiki/Carbon_dioxide;
3)https://it.wikipedia.org/wiki/Effetto_serra
4)BASI DI ECOLOGIA – ODUM -1988 -PICCIN
Figura_1 equilibri del biossido di carbonio in acqua.
Figura_2 reazione tra il biossido di carbonio con il calcare.
Figura_3 The Keeling Curve of atmospheric CO2 concentrations measured at Mauna Loa Observatory
By Delorme – Own work. Data from Dr. Pieter Tans, NOAA/ESRL and Dr. Ralph Keeling, Scripps Institution of Oceanography., CC BY-SA 4.0, https://commons.wikimedia.org/w/index.php?curid=40636957
Figura_4 Annual (thin lines) and five-year lowess smooth (thick lines) for the temperature anomalies averaged over the Earth’s land area and sea surface temperature anomalies (blue line) averaged over the part of the ocean that is free of ice at all times (open ocean).
By NASA – https://data.giss.nasa.gov/gistemp/graphs/, Public Domain, https://commons.wikimedia.org/w/index.php?curid=63276564



